Gastrointestinal (GİS) sistem, ağızdan başlayarak anüse kadar uzanan ve besinlerin sindirimi, emilimi ve atılımından sorumlu olan oldukça karmaşık bir organlar bütünüdür. Bu geniş anatomik hat boyunca gelişen malign (kötü huylu) tümörler, dünya genelinde kanser kaynaklı ölümlerin en önemli nedenleri arasında yer almaktadır. Gastrointestinal sistem kanserleri, çok katmanlı epitel dokulardan köken alan ve erken dönemde sinsi ilerleyebilen bir yapıya sahiptir. Günümüzde onkolojik cerrahi, bu kanserlerin tedavisinde küratif (iyileştirici) amacın temel taşını oluşturmaktadır.
Tıbbi terminolojide "digestive tract" olarak adlandırılan bu sistemdeki kanserleşme süreçleri; cerrahinin yanı sıra tıbbi onkoloji, radyasyon onkolojisi, gastroenteroloji ve radyoloji disiplinlerinin bir arada çalıştığı multidisipliner bir yönetimi zorunlu kılar. Modern tıbbın sunduğu teknolojik imkanlar, cerrahi müdahalelerin başarısını artırırken, hasta sağkalım oranlarını ve yaşam kalitesini doğrudan etkilemektedir. Bu rehberde, gastrointestinal kanserlerin patofizyolojisinden cerrahi inovasyonlara kadar tüm süreçler, bilimsel veriler ışığında ele alınacaktır.
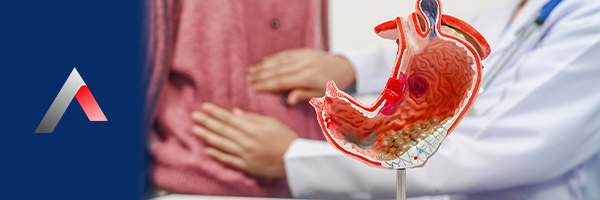
Gastrointestinal kanser nedir sorusuna tıbbi bir perspektifle yanıt vermek gerekirse; bu durum sindirim kanalını oluşturan organların duvar katmanlarındaki hücrelerin, genetik mutasyonlar sonucu kontrolsüz bir şekilde çoğalmasıdır. Gastrointestinal sistem; özofagus (yemek borusu), mide, ince bağırsak, kolon (kalın bağırsak), rektum, anüs, pankreas, karaciğer ve safra yollarını kapsar.
Hücresel düzeyde süreç genellikle mukoza tabakasındaki epitelyal hücrelerde başlar. Sağlıklı bir hücrenin DNA yapısı bozulduğunda, hücre normal ölüm döngüsüne (apoptozis) girmek yerine kontrolsüzce bölünmeye devam eder. Bu birikim sonucunda "tümör" adı verilen kitleler oluşur. Eğer bu kitleler çevre dokulara sızma (invazyon) ve kan/lenf yoluyla uzak organlara yayılma (metastaz) yeteneği kazanırsa, süreç malignite yani kanser olarak tanımlanır.
Gastrointestinal sistemin iç yüzeyi sürekli olarak kimyasal, mekanik ve mikrobiyolojik etkenlere (mide asidi, safra, gıdalardaki karsinojenler, bakteriler) maruz kaldığı için, bu bölgedeki hücrelerin yenilenme hızı yüksektir. Ancak bu hızlı döngü, hatalı DNA eşleşmeleri riskini de beraberinde getirir. Gastrointestinal sistem kanserleri, patolojik olarak çoğunlukla "adenokarsinom" tipindedir; yani salgı yapan bez hücrelerinden köken alırlar. Tanı konulurken kanserin hangi katmana kadar ilerlediği (T evresi), lenf nodu tutulumu (N evresi) ve uzak organ sıçraması (M evresi) dikkate alınarak TNM sınıflaması yapılır.
Gastrointestinal sistemde yer alan her organın kendine has bir histolojik yapısı ve dolayısıyla farklı kanser türleri mevcuttur.
Dünya genelinde en sık görülen GİS kanserlerinden biridir. Özellikle Helicobacter pylori enfeksiyonu, tütsülenmiş gıdalar ve genetik yatkınlık temel risk faktörleridir. Adenokarsinomlar, mide kanserlerinin yaklaşık %90-95'ini oluşturur. Prevalans verilerine göre erkeklerde kadınlara oranla daha sık izlenir.
Genellikle poliplerden köken alan bu kanser türü, erken teşhis ile önlenebilir kategorisindedir. Batı tipi beslenme ve sedanter yaşam risk artışına neden olur. Kolorektal kanserler, dünya genelinde kanser kaynaklı ölümlerde üçüncü sırada yer almaktadır.
GİS kanserleri içinde en agresif seyreden türdür. Pankreasın ekzokrin hücrelerinden (duktal adenokarsinom) veya nöroendokrin hücrelerinden gelişebilir. Sinsi seyri nedeniyle genellikle ileri evrede saptanır; bu nedenle cerrahi teknikler (Whipple ameliyatı gibi) büyük uzmanlık gerektirir.
Sıklıkla kronik Hepatit B, Hepatit C veya siroz zemininde gelişir. Primer karaciğer kanserlerinin yanı sıra, karaciğer diğer GİS kanserlerinin metastazı için de en sık hedef olan organdır.
Yassı hücreli karsinom (squamous) ve adenokarsinom olmak üzere iki ana tipe ayrılır. Alkol, sigara kullanımı ve kronik reflüye bağlı gelişen Barrett özofagusu başlıca nedenlerdir.
Nispeten daha nadir görülürler. İnce bağırsak kanserleri genellikle karsinoid tümörler veya lenfomalar şeklinde karşımıza çıkarken; anüs kanserleri çoğunlukla HPV (Human Papilloma Virus) ile ilişkilidir.
Gastrointestinal kanserler, gelişim aşamalarında genellikle özgün olmayan, gündelik sindirim sorunlarıyla karıştırılabilecek belirtiler verir. Bu durum, hastalığın "sinsi" karakterini oluşturur. En sık karşılaşılan semptomlar şunlardır:
Açıklanamayan Kilo Kaybı: İştahsızlık olmasa dahi vücut kitle indeksindeki ani düşüş.
Anemi ve Halsizlik: Tümörün kronik olarak mikroskobik düzeyde kanaması sonucu gelişen demir eksikliği.
Dışkılama Alışkanlığında Değişiklik: İshal veya kabızlık atakları, dışkı formunda incelme.
Karın Ağrısı ve Şişkinlik: Sindirim sistemindeki tıkanıklıklara veya periton (karın zarı) irritasyonuna bağlı huzursuzluk.
Yutma Güçlüğü (Disfaji): Özellikle özofagus kanserinde belirgindir.
Melen (Siyah Dışkı): Üst sindirim sistemi kanamalarının bir göstergesidir.
Nedenleri arasında genetik yatkınlık (Lynch Sendromu, FAP), kronik inflamatuar bağırsak hastalıkları (Crohn, Ülseratif Kolit), obezite, tütün ürünleri, aşırı alkol tüketimi ve işlenmiş et ürünlerinden zengin diyet yer almaktadır. Erken teşhis, bu belirtilerin ciddiye alınması ve tarama programlarına katılım ile mümkündür.
Modern onkolojide kesin tanı ve evreleme için ileri teknolojik görüntüleme ve biyopsi teknikleri bir arada kullanılır. Gastrointestinal kanser tanı yöntemleri, hastalığın yayılımını milimetrik düzeyde saptamayı hedefler.
Endoskopi ve Kolonoskopi: Ucunda kamera bulunan esnek borularla sindirim sisteminin doğrudan incelenmesi işlemidir. Şüpheli alanlardan "forceps" aracılığıyla parça alınmasını (biyopsi) sağlar. Altın standarttır.
EUS (Endoskopik Ultrason): Endoskopi ucuna yerleştirilmiş bir ultrason probu ile organ duvarlarının katmanlarını ve komşu lenf bezlerini inceleme yöntemidir. Özellikle mide ve pankreas kanserlerinin evrelenmesinde kritiktir.
PET-BT (Pozitron Emisyon Tomografisi): Vücuda verilen radyoaktif işaretli şekerin (FDG) kanserli hücreler tarafından tutulmasını izler. Metastazların tespiti ve tedavi başarısının ölçülmesinde kullanılır.
MR (Manyetik Rezonans) ve BT: Karaciğer tümörleri ve pelvik bölgedeki rektum kanserlerinin anatomik detaylarını, damar ilişkilerini ortaya koymak için kullanılır.
Sıvı Biyopsi: Henüz rutin kullanıma yeni giren bu yöntemle, kanda dolaşan tümör DNA'sı (ctDNA) analiz edilerek erken teşhis ve nüks takibi yapılabilmektedir.
A Life Sağlık Grubu ve benzeri tam teşekküllü merkezlerde, bu yöntemlerden elde edilen veriler radyologlar ve patologlar tarafından titizlikle analiz edilerek hastaya özel tedavi haritası çıkarılır.
GİS kanserlerinde cerrahi, tümörün tamamen vücuttan uzaklaştırılmasını (R0 rezeksiyon) amaçlar. Günümüzde cerrahi müdahaleler, "minimal invaziv" tekniklere doğru evrilmiştir.
Laparoskopik ve Robotik Cerrahi
Geleneksel açık cerrahinin aksine, karın bölgesine açılan küçük deliklerden (trokar) girilerek yapılır. Robotik cerrahi (Da Vinci), cerraha 3 boyutlu derinlik ve el bileğinden daha esnek hareket kabiliyeti sunar. Bu yöntemler; daha az kanama, daha az ağrı ve daha hızlı iyileşme süreci sağlar.
HIPEC (Sıcak Kemoterapi)
Özellikle karın zarına yayılmış (peritoneal karsinomatozis) mide ve kolon kanserlerinde, gözle görülen tüm kitleler temizlendikten sonra karın boşluğuna 42 dereceye kadar ısıtılmış kemoterapötik ilaçların uygulanmasıdır. Isı, ilacın tümör hücrelerine nüfuzunu artırır.
PIPAC (Basınçlı Aerosol Kemoterapi)
Cerrahi şansı olmayan veya yaygın periton tutulumu olan hastalarda, kemoterapinin karın içine basınçlı sprey (aerosol) şeklinde uygulanmasıdır. Laparoskopik olarak gerçekleştirilen bu yöntem, sistemik yan etkileri azaltırken yerel kontrol sağlar.
Multidisipliner Yaklaşım: Tümör Konseyi
Modern onkolojik yaklaşımda hiçbir cerrah tek başına karar vermez. Cerrahi onkolog, tıbbi onkolog, radyasyon onkoloğu, gastroenterolog ve radyologdan oluşan Tümör Konseyi, her hastanın dosyasını bireysel olarak inceler ve en uygun tedavi sıralamasını (neoadjuvan/ameliyat öncesi veya adjuvan/ameliyat sonrası tedavi) belirler.
| Özellik | Klasik Açık Diskektomi | Mikrocerrahi (Mikrodissektomi) |
|---|---|---|
| Kesi Boyutu | 5 - 8 cm | 1.5 - 2.5 cm |
| Görüntüleme | Çıplak göz veya büyüteç | Yüksek çözünürlüklü mikroskop |
| Kas Hasarı | Daha fazla (kas sıyırma) | Minimal (doku koruyucu yaklaşım) |
| Hastanede Kalış | 2 - 3 gün | 1 gün (genellikle aynı gün taburcu) |
| İyileşme Süresi | 4 - 6 hafta | 1 - 2 hafta |
Gastrointestinal cerrahi sonrası iyileşme dönemi, uygulanan yönteme ve organın fonksiyonuna göre değişkenlik gösterir. Modern protokoller (ERAS - Enhanced Recovery After Surgery), hastanın ameliyat sonrası en kısa sürede ayağa kalkmasını ve beslenmeye başlamasını hedefler.
Hastanede kalış süresi laparoskopik vakalarda 3-5 gün, robotik cerrahide ise benzer sürelerdedir. İlk etapta sıvı beslenme ile başlayan süreç, diyetisyen kontrolünde kademeli olarak katı gıdaya geçer. Ameliyat sonrası dönemde dren takibi, yara bakımı ve gerekirse evde bakım hizmetleri, A Life Sağlık Grubu uzmanlığında titizlikle yürütülür. Hastaların uzun dönemde belirli aralıklarla tümör markerları (CEA, CA 19-9) ve görüntüleme yöntemleriyle takibi hayati önem taşır.
Fiyatlarımız ve Uygulama Yöntemlerimiz Hakkında Hızlı Bilgi Alma Formumuzu Kullanabilirsiniz.
GİS kanserleri genellikle 4 evreye ayrılır. Evre 1 tümörün organ duvarında sınırlı olduğu, Evre 4 ise karaciğer veya akciğer gibi uzak organlara yayıldığı aşamadır. Evreleme, tedavi yöntemini belirleyen en temel unsurdur.
Ameliyat süresi; tümörün yerleşim yerine, evresine ve seçilen yönteme (açık, kapalı, robotik) göre 2 ile 8 saat arasında değişebilir. Örneğin bir rektum kanseri ameliyatı ortalama 3-4 saat sürerken, Whipple ameliyatı daha uzun sürebilir.
Sindirim sistemi ameliyatlarından sonra mide ve bağırsakların yeni düzene alışması için az ve sık beslenme (damping sendromunu önlemek adına) önerilir. Yüksek proteinli, lifli ve işlenmiş şekerden uzak bir diyet tercih edilmelidir.
Özellikle ailesinde birden fazla kanser öyküsü olan genç hastalarda, Lynch sendromu veya genetik mutasyonların tespiti için genetik danışmanlık ve testler önerilmektedir.
Çoğu hastada uygulanabilse de, tümörün çok büyük olması, komşu organları tamamen sarması veya hastanın daha önce geçirdiği çok sayıda karın ameliyatı nedeniyle gelişen yapışıklıklar kapalı cerrahiye engel teşkil edebilir.
Robotik cerrahi, özellikle pelvis gibi dar alanlarda (rektum kanseri cerrahisi) sinir koruyucu cerrahi yapılmasına olanak tanıyarak ameliyat sonrası cinsel fonksiyonların ve idrar kontrolünün korunmasında daha başarılı sonuçlar verebilir.
7/24 tüm soru ve sorunlarınız için buradayız.